Fabryho choroba
Vloženo 30.12.2019 , poslední aktualizace 25.11.2022
Obsah
Etiopatogeneze
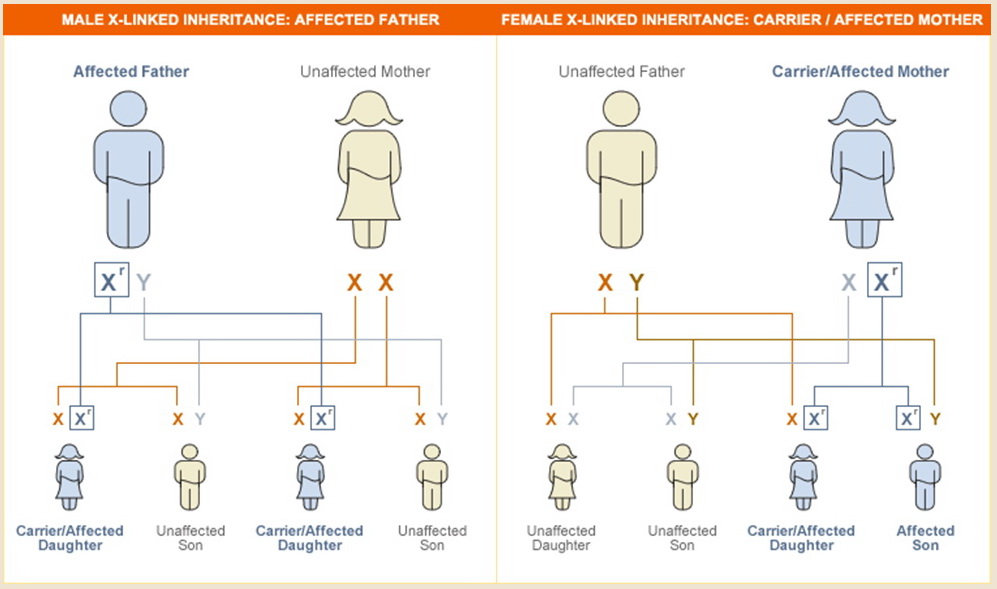
- Fabryho choroba je vázaná na chromozom X
- muži s Fabryho chorobou předávají defektní gen všem svým dcerám, synové jsou zdrávi
- ženy mají 50% pravděpodobnost, že gen svým dětem předají
- muži s Fabryho chorobou předávají defektní gen všem svým dcerám, synové jsou zdrávi
- mutace genu pro α‑galaktosidázu A (α‑Gal‑A), lokalizovaného na na chromosomu X
- známo > 400 jeho mutací, které způsobují úplný nebo částečný defekt lyzosomálního enzymu α‑Gal‑A, který odpovídá za štěpení glykosfingolipidů
- jeho substrát – především globotriaosylceramid (Gb3) se nemůže odbourávat jinými cestami a hromadí se v lyzosomech – tím postihuje buněčné funkce a způsobuje orgánové komplikace
- hlavní postižené buňky
- cévní endotelie a buňky hladkého svalstva cév
- buňky ledvin
- buňky myokardu
- nervové buňky
- vliv pohlaví na průběh choroby
- postižení je větší u mužů větší a projevuje se dříve – muži jsou hemizygoti a choroba se u nich chová jako dominantní
- u žen je vždy jeden z chromosomů X inaktivován (lyonizace) – ženské tělo je tak mozaikou složenou z buněk, v nichž je aktivní buď zdravý nebo nemocný chromosom X. Na rozdíl od jiných chorob vázaných na chromosom X, jako jsou třeba hemofilie, není populace buněk s exprimovaným zdravým chromosomem schopna korigovat metabolický defekt buněk, kde je aktivní chromosom nesoucí mutaci genu. V těchto buňkách pak dochází ke střádání a orgánové projevy se mohou podle množství postižených buněk blížit těm, které jsou přítomny u mužů
CMP vznikají v důsledku:
- dolichoektazie
- kardioembolizace
- arteriolopatie
Bez léčby nemocní umírají po 40. roce věku
Klinický obraz
Nefropatie
- od 2. decenia, progresivní – způsobena postižením buněk glomerulů a tubulů
- objevuje se mikroalbuminurie a posléze proteinurie
- především u mužů pak onemocnění progreduje postupným poklesem GF až do stadia renálního selhání s nutností dialyzační terapie nebo transplantace ledvin
- osud transplantované ledviny je u Fabryho choroby dobrý, neboť v ní již ke střádání nedochází
- diagnóza onemocnění je nezřídka stanovena díky renální biopsii provedené pro nález proteinurie
- při klasické fixaci bioptického materiálu však v buňkách nemusejí být patrny lipidové inkluze, které jsou rozpuštěny a zbývá po nich jen vakuolizace
- klasickým obrazem v elektronovém mikroskopu jsou zebrovitá tělíska akumulovaného Gb3
Kardiologické obtíže
- postižení velmi komplexní – střádání je prokazatelné nejen v endoteliálních buňkách arteriol a kapilár, ale rovněž v buňkách hladkého svalstva cév.
- snížení koronární rezervy, endoteliální dysfunkce a ischémie, kardiomyopatie a fibrosa myokardu ⇒ kardiální selhání
- arytmie
- poruchy převodu ve formě raménkových blokád nebo AV blokád různého stupně. Tito nemocní vyžadují implantaci trvalého kardiostimulátoru. Ten však potřebují i ti, u nichž se vyvine pro chorobu celkem typická chronotropní inkompetence, která brání pacientům zvýšit tepovou frekvenci při zátěži, a zhoršuje tak jejich dušnost
- fisi a flutter síní ⇒ kardioembolizace
Diagnostika
Klinický obraz
- „kryptogenní“ iCMP/TIA v mladém věku + nefropatie + neuropatie + kardiopatie
- kožní a oční léze (viz výše)
Terapie
Obsah dostupný pouze pro přihlášené předplatitele.
V České republice je péče koncentrována na II. interní kliniku kardiologie a angiologie 1. LF UK a VFN v Praze, kam je rovněž možno nemocné adresovat při podezření na tuto diagnózu. Dg je ověřena jednak stanovením koncentrace α‑galaktosidázy (může selhávat u žen, u kterých mohou být hodnoty jen mírně sníženy) a genetickým testováním.