ISCHEMICKÉ CMP / KLASIFIKACE A ETIOPATOGENEZE / HYPERKOAGULAČNÍ STAVY
Hyperkoagulační stavy (trombofilie)
Vloženo 08.01.2020 , poslední aktualizace 06.09.2021
Obsah
-
žilní trombóza – dominuje oblenění toku a hyperkoagulace, ke které dochází při aktivaci plazmatických koagulačních faktorů a selhání funkce jejich inhibitorů v plazmě a cévní stěně
-
arteriální trombóza – spíš aktivace a agregace trombocytů a dysfunkce endotelu (většinou v důsledku AS)
Trombofilie
- zvýšená dispozice ke vzniku trombů (vrozená, získaná)
-
klinická manifestace bývá především u homozygotních forem, u heterozygotní formy je ke klinické manifestaci třeba kumulace dalších cévních rizikových faktorů
-
přítomnost těchto mutací u pacientů s iCMP je obdobná jako u zdravé populace
-
deficit AT III 5%, deficit PS 0.9% [Hankey, 2001]
-
-
k celkovému riziku trombembolie přispívá přítomnost dalších rizikových faktorů:
- vaskulární rizikové faktory
- imobilizace / peroperační stavy
- gravidita / užívání HAK
- současné nádorové onemocnění (získaný hyperkoagulační stav)
- například heterozygoti s Leidenskou mutací mají 5-10x vyšší relativní riziko vzniku trombotických komplikací, uživání HAK či hormonální substituční léčby u heterozygotů s Leidenskou mutací pak toto riziko zvyšuje až na 35ti násobek oproti zdravé populaci a riziko může být až 100 násobné při přítomnosti dalších mutací (faktor II, MTHFR)
Klasifikace
| Mechanismy podílející se na vzniku iCMP |
| Deficit faktorů inhibujících koagulaci (AT III, PC a PS) Zvýšená hladina koagulačních faktorů (typicky V a VII) Snížená fibrinolytická aktivita (deficit plasminogenu a inhibice aktivátoru plasminogenu) |
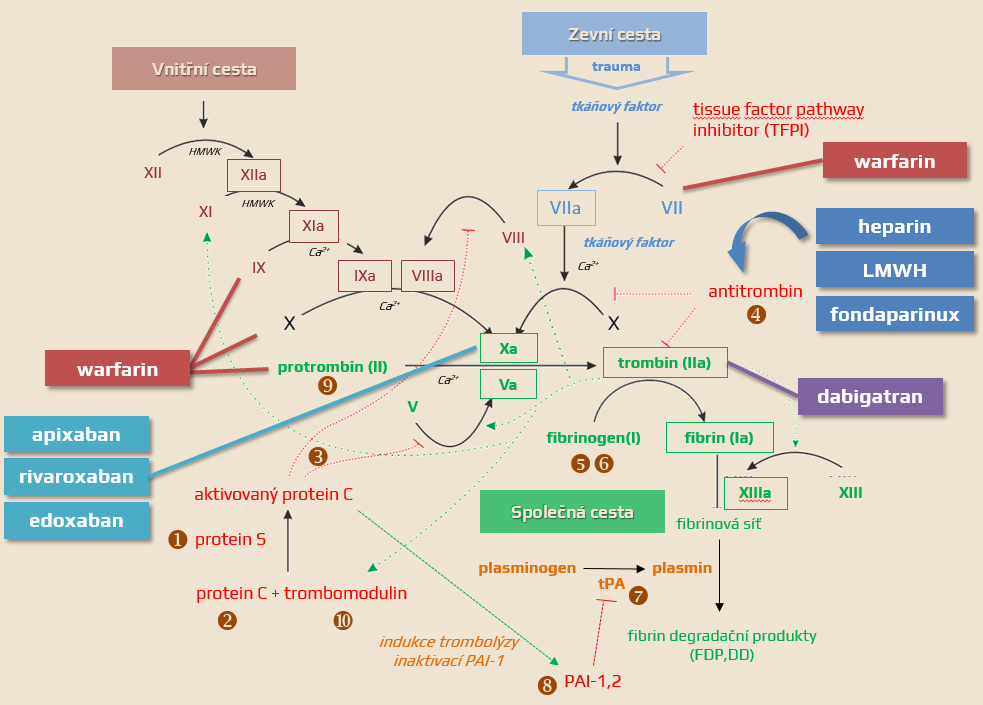
Obsah dostupný pouze pro přihlášené předplatitele.
Diagnostika
Biochemické a hematologické vyšetření
Obsah dostupný pouze pro přihlášené předplatitele.
Přehled hyperkoagulačních stavů
Deficit proteinu S |
- protein S je kofaktorem aktivovaného proteinu C (APC), který reguluje přeměnu protrombinu na trombin
- vzácná heterogenní skupina onemocnění (více než 130 různých genových mutací)
- výskyt:
- v běžné populaci 0,01-0,1 %
- u pacientů s prodělanou DVT v 2,3-4,6 %
- RR DVT až 10x vyšší u asymptomatických jedinců oproti běžné populaci
- RR rekurence DVT ~ 1,5-3 násobné zvýšení (roční riziko rekurence DVT zpočátku ~ 15%)
| Získané příčiny deficitu proteinu S |
|
Mutace faktoru II – protrombin 20210A |
- 2. nejčastější vrozená trombofilie vzniká na podkladě záměny glutaminu za arginin v nukleotidové pozici 20210
- defekt vede k vyšším koncentracím faktoru II – protrombinu, a tím zvyšuje riziko vzniku trombózy
- zvýšení rizika rekurence DVT v přítomnosti této mutace je nejasné a pravděpodobně izolovaná heterozygotní mutace nemá vliv na vznik rekurence DVT
- doporučení v délce antikoagulační léčby a v prevenci tromboembolismu v těhotenství jsou shodná jako u heterozygotní mutace faktoru V Leiden.
- v případě kombinace 2 mutací (heterozygot pro faktor V Leiden + faktor II – protrombin) je riziko rekurence hluboké žilní trombózy již 2-5násobně zvýšené
- je doporučena antikoagulační léčba po dobu 12 měsíců (úroveň doporučení 1C+)
- dlouhodobá antikoagulační léčba zůstává v třídě 2C.
Deficit tPA |
- nezávislý rizikový faktor IM a iCMP
- největší část tPA cirkuluje jako inaktivovaný komplex s inhibitorem aktivátoru plasminogenu (PAI-1)
- snížená koncentrace tPA snižuje fibrinolytickou aktivitu a urychluje aterosklerózu (zejména krkavic a periferních cév )
Hyperfibrinogenémie |
- zvýšená hladina fibrinogenu zvyšuje riziko iktu (nezávislý faktor)
- zvýšení viskozity krve, agregability destiček, podporuje aterogenezi a účastní se na formování trombu
- dlouhodobé snížení jeho hladin nevede ke snížení rizika iCMP
Hyperhomocysteinémie a mutace metylentetrahydrofolát reduktázy |
Obsah dostupný pouze pro přihlášené předplatitele.
Zvýšená koncentrace koagulačních faktorů |
- nejvýznamnější je faktor VIII
- vzestup aktivity > 150 % vede ke zvýšení relativního rizika vzniku DVT až 5x
- lehce zvyšuje i riziko arteriální trombózy Kamphuisen,2001]
- stejně důležité je i ↑ hladiny fibrinogenu, které vede ke zvýšení rizika DVT 4x

