DOPLŇKY / MEDIKACE / ANTIKOAGULACE
Praxbind (idarucizumab)
Vloženo 20.09.2019, poslední aktualizace 10.11.2021
Obsah
- použití idarucizumabu jako antidota bylo schváleno FDA v říjnu 2015 [Cassels, 2015]
- má 300x vyšší afinitu k trombinu než dabigatran
- je indikován u dospělých pacientů léčených přípravkem dabigatran (PRADAXA) v situacích, kdy je třeba urychleně zvrátit jeho antikoagulační účinky:
- při naléhavých chirurgických/urgentních výkonech (k urgentním výkonům patří i trombolýza)
- při život ohrožujícím nebo nekontrolovaném krvácení (vč. ICH)
- nejsou prakticky žádné kontraindikace (kromě alergie) ani relevantní lékové interakce, žádné závažné NÚ
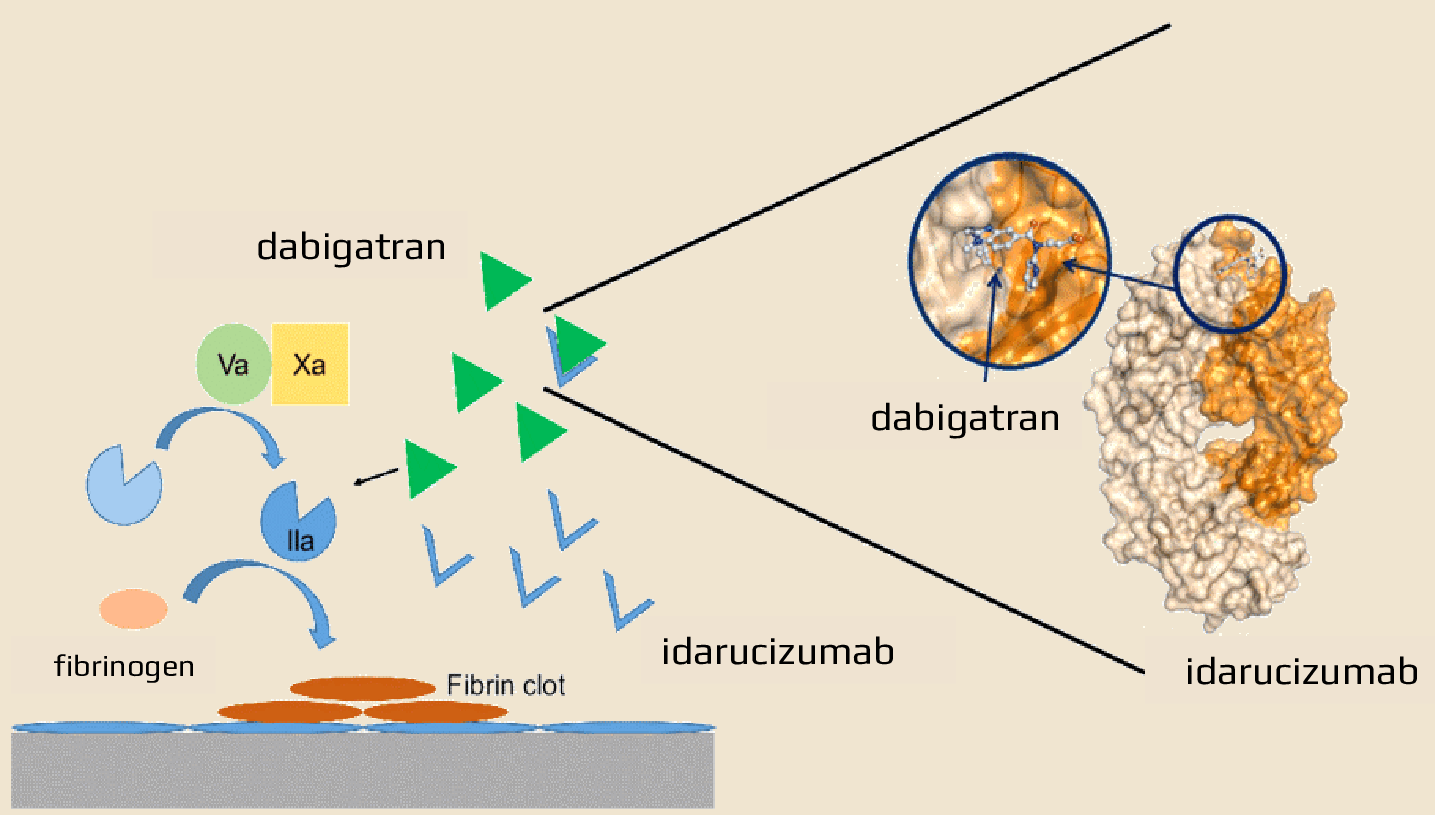
Mechanismus účinku
- idarucizumab je fragment humanizované monoklonální protilátky
- pevně se váže na dabigatran a vytvoří s ním komplex, čímž se protisrážlivý účinek dabigatranu ihned zastaví (dabigatran má k idarucizumabu 300x vyšší afinitu než k trombinu)
- neruší účinky jiných antikoagulancií
- nevede k hyperkoagulačnímu stavu
- rychlé IV podání s rychlým nástupem účinku
- umožňuje rychlý restart antikoagulační terapie (24h po jeho podání)
Klinické studie
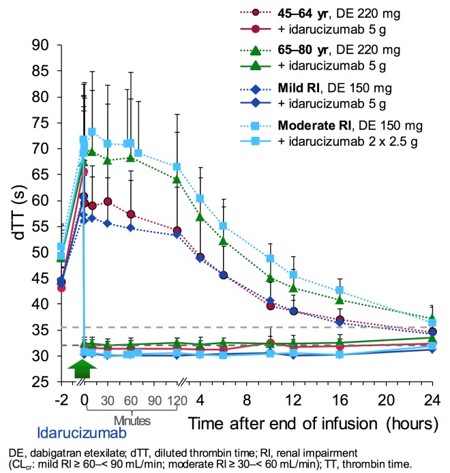
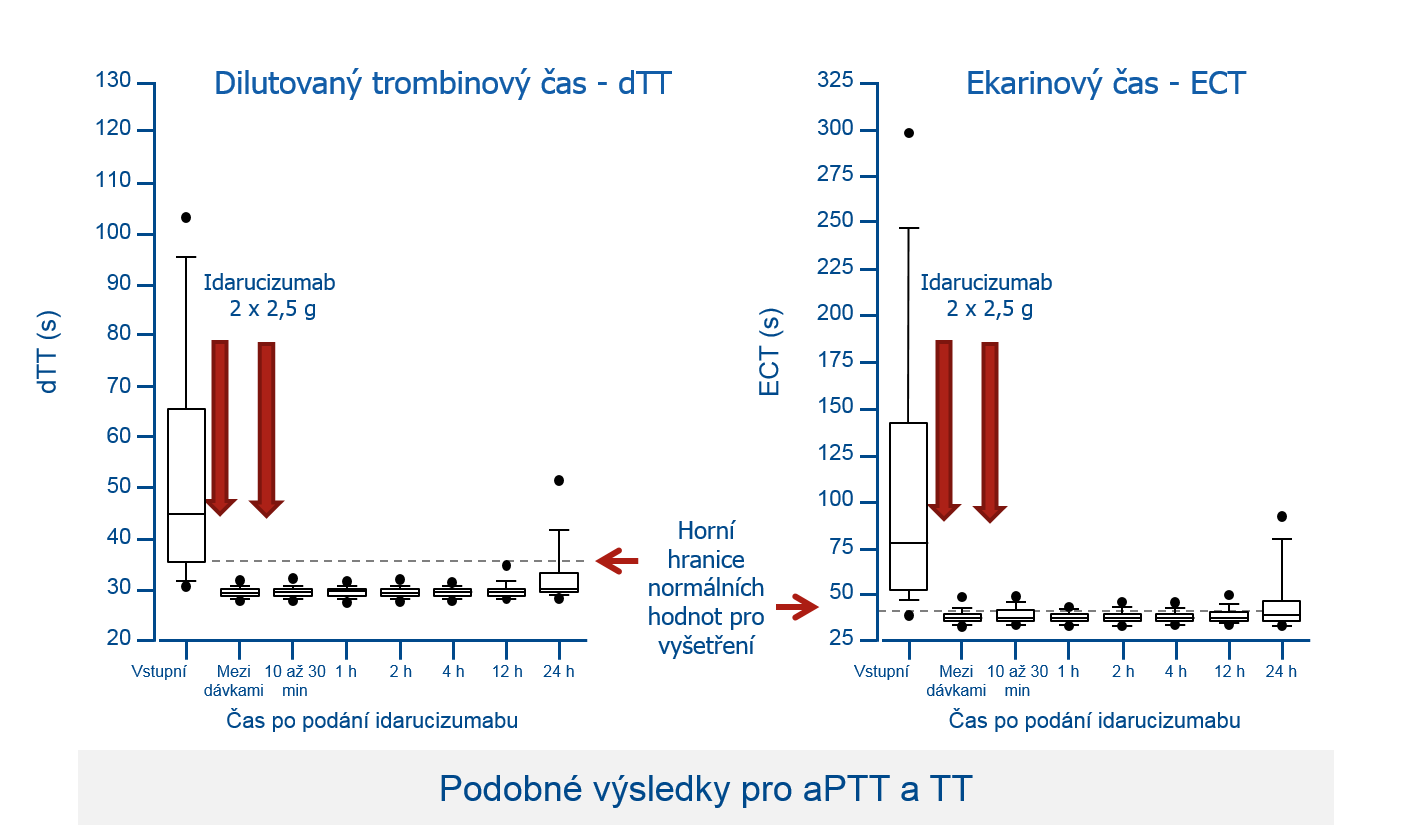
- studie RE-VERSE AD s i.v. antidotem idarucizumabem v dávce 5g i.v.
- účinek během pár minut
- analýza 90 pacientů prokázala spolehlivou redukci antikoagulační aktivity (po 4 a 12 h normální koagulace u 90% pacientů) → viz zde
- množí se klinické zkušenosti s podání PRAXBINDu před trombolýzou a u akutních ICH → viz zde
Kontraindikace a omezení
- alergie na idarucizumab nebo jeho složky
- pacienti s dědičnou intolerancí fruktózy mohou být ohroženi nežádoucími účinky (např. nízkou hladinou cukru v krvi, nízkou hladinou fosfátů, metabolickou acidózou, zvýšením kyseliny močové a akutním selháním jater).
- u těhotných žen nejsou kontrolované studie a není známo, zda idarucizumab může způsobit poškození plodu
- nebylo studováno použití během porodu a krátce po porodu
- není známo, zda a v jakém množství přechází idarucizumab do mateřského mléka
- není znám efekt na kojené dítě
- zvažit přínosy kojení versus význam podání léčiva u matky (risk-benefit)
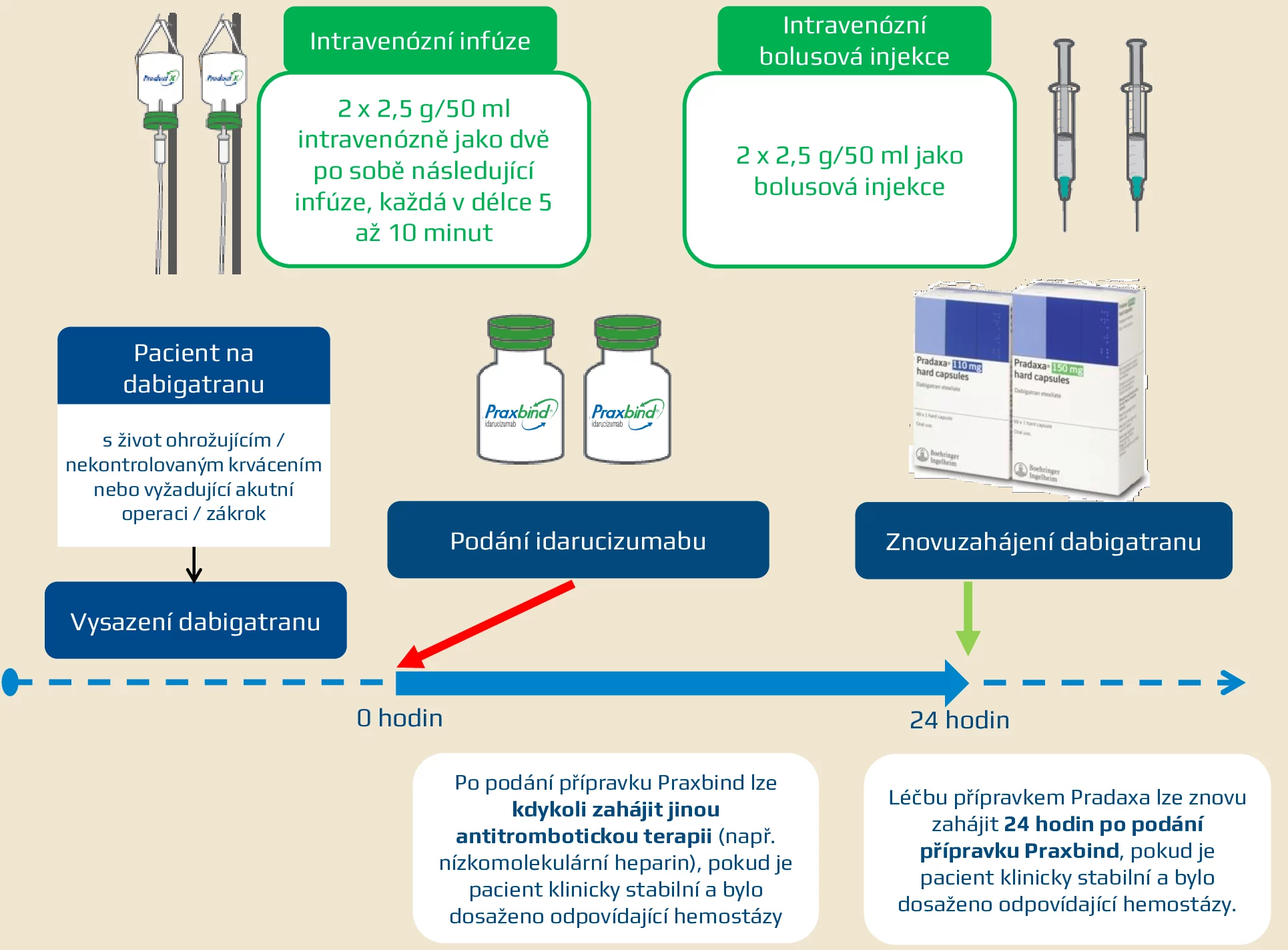
Dávkování
- PRAXBIND 2 x 2.5g/50 ml – rychlá infúze (2 infúze po sobě, každá cca 5min) nebo bolusové pomalé injekční podání
- lze použít stávající intravenózní linku, kterou je nutné před a po infúzi propláchnout 0,9% roztokem NaCl
- stejnou linkou nepodávat žádné jiné infúze
- za 24h lze dle potřeby opět zahájit antikoagulaci
Praxbind a intravenózní trombolýza
- trombolýza u pacientů s akutní ischemickou CMP je při léčbě dabigatranem možná, pokud hodnoty aPTT a TT, ECT nebo HEMOCLOTu) nepřesahují horní hranice referenčních hodnot (AHA/ASA 2013 III/C)
- pouze aPTT nestačí, normální APTT zcela nevylučuje patologický TT [Kermer, 2017] [Hankey, 2014]
- IVT možné zvážit u pacientů s normálním TT , APTT a PT
- u Hemoclotu hladina dabigatranu < 50ng/ml > 6h od podání poslední dávky léku značí absenci antikoagulační aktivity
- SPC – použití fibrinolytik při léčbě akutní iCMP lze zvážit u pacientů s hodnotami dTT (dilutovaný trombinový čas), ECT (ecarinový test) nebo aPTT (aktivovaný parciální tromboplastinový čas) nepřesahujícími horní hranice normy místních referenčních hodnot
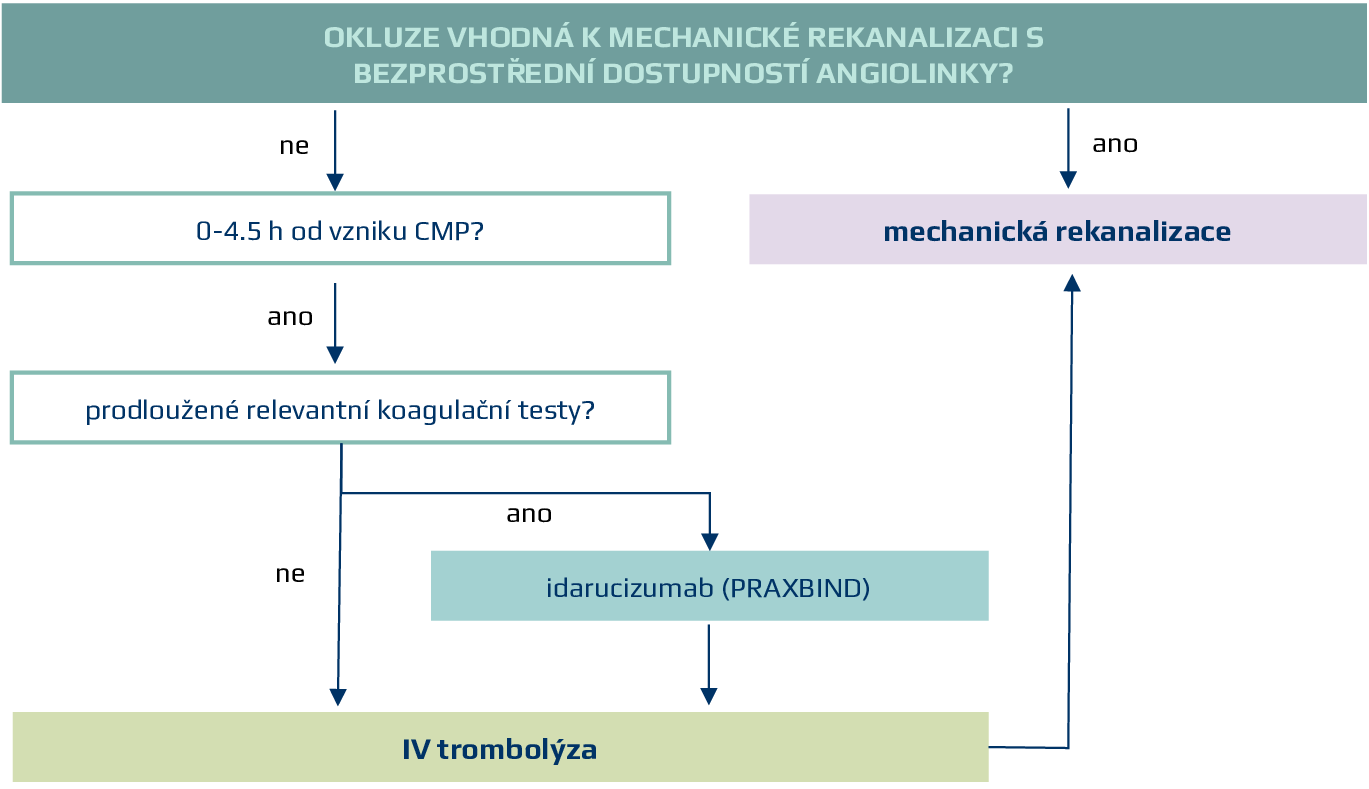
- podání trombolýzy do 4.5h od vzniku CMP po předchozím zrušení efektu dabigatranu antidotem PRAXBIND je možné (mezi indikace Praxbindu patří urgentní procedury, mezi které lze počítat i trombolýzu)
- lze se opřít o názor expertů (ESO guidelines 2021) [Diener, 2017]
- postup je podpořen konsensem CVS → viz zde
- dle údajů z registrů je podání antidota PRAXBIND u pacientů s akutní CMP a následným podáním trombolýzy efektivní, bezpečené a snadno proveditelné [Kermer, 2017]
- studie s dabigatranem po 4.5 hodině (např. trombolýza dle CTP) nejsou k dispozici a v guidelines tato situace není zmíněna
Nežádoucí účinky
- běžné nežádoucí účinky
- hypokalémie (7 %)
- delirium (7 %)
- zácpa (7 %)
- horečka (6 %)
- zápal plic (6 %)
- bolest hlavy (5 %)
- závažné nežádoucí účinky
- zvýšené riziko trombembolie při základním onemocnění, pro které je dabigatran podáván (idarucizumab ale nevyvolává hyperkoagulační stav)
- recidiva krvácení (někteří pacienti mohou potřebovat další dávku idarucizumabu)
- alergická reakce (horečka, dýchací potíže způsobené stažením dýchacích cest, hyperventilace, vyrážka a svědění)
- pacienti s dědičnou intolerancí fruktózy mohou být ohroženi nežádoucími reakcemi, jako je hypoglykémie, hypofosfatémie, metabolická acidóza, zvýšení kyseliny močové a akutní selhání jater